水に難溶なアニリンに塩酸を加えると、アニリン塩酸塩として水に溶ける(式1)。 酢酸ナトリウムを加えると平衡反応で、アニリンと酢酸が発生する(式2)。 発生したアニリンは、水溶液中の無水酢酸とすぐに反応してアセトアニリドになる(式3)。 5無水酢酸は,主 として酢酸セルロースの製造に使われ るほか,医 薬品,香 料,染 料,可 塑剤,農 薬,そ の他の 有機合成品の原料として,工 業上有用な化合物であり, その工業的製法としては,従 来,ケ テン法*1,お よびア セトアルデヒド酸化法*2が 代表的なものとして知られて いる。 一方,酢 酸メチルベンゼン環にアミノ基が結合した化合物であり、最も単運な芳香族アミンである。 構造式 性質 有毒で無色の液体。特異的な匂いがする。 酸化すると褐色に変化する。 弱塩基性 を示す。 水には溶けにくいが、塩基であるため塩酸に

アセトアニリド Wikipedia
アニリン 無水酢酸 反応式
アニリン 無水酢酸 反応式-®塩酸と反応し、アニリン塩酸塩を生じる。c h nh hcl c h nh cl65 2 6 5 3→ - ß無水酢酸ともに加熱するとアセトアニリドができる。(アセチル化) +( ) +ch co o ch cooh 3 2 → 3 無水酢酸 c h nhcoch 65 3 アセトアニリド中の 結合をアミド結合といい、この結合をもつ化合物を総称してnhcoアミドという無水酢酸 31ml × 1069(g/ml) / 102g/mol = mol 酢酸ナトリウム・三水和物 40(g) / (54)g/mol = mol よって限定反応物質はアニリンになる。すなわち、アニリンと等モルのアセトアニリドできることになる。
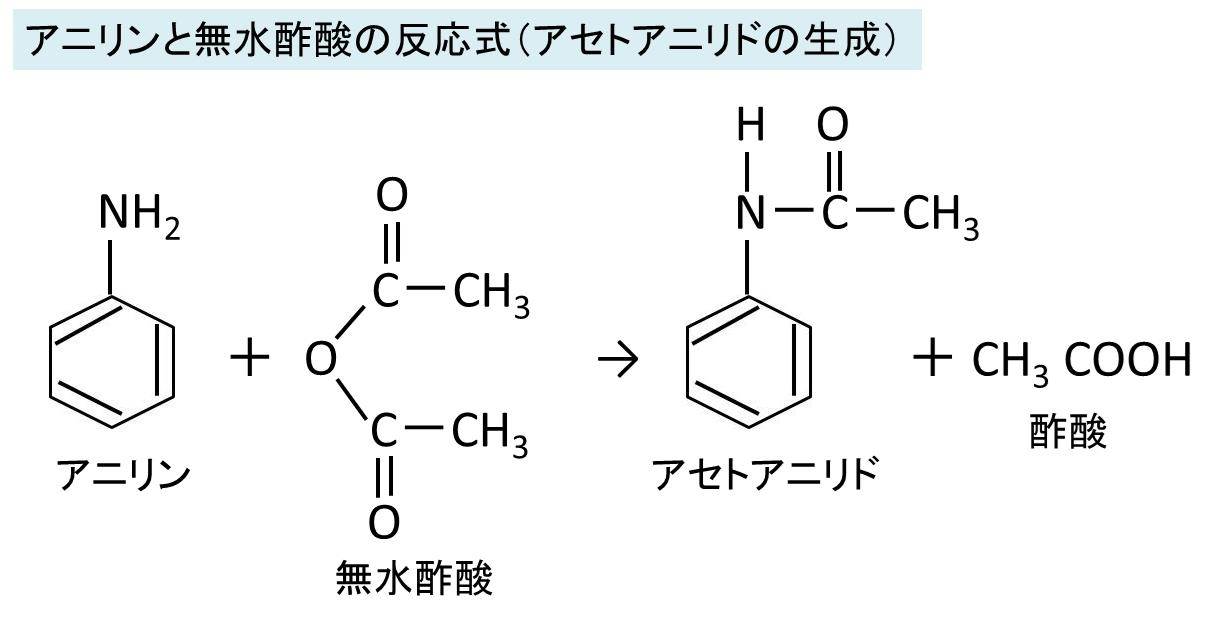



アニリンと無水酢酸の反応式 アセトアニリド生成 酢酸を使用しない理由は
アニリンと無水酢酸の反応式 アセトアニリド生成 酢酸を使用しない理由は アニリンの反応 生徒実験 じぃの科学だいすきブログ アニリンの性質と製法 塩化ベンゼンジアゾニウムとpヒドロキシアゾベンゼン Irohabook アセトアニリドのアミド化による合成法を暗記0にする方法 化学受験目的 アニリンと無水酢酸との反応により,アセトアニリドが生成すること(アセチル化反応)を学 ぶ.また,その収率を求める. 解説 1.アセトアニリド 人工的に作られた最初の合成解熱剤がアセトアニリドであり,以前はアンチフェブリン (Antifebrin)の名称で呼ばれた.1853年に仏の分子式:c 4 h 6 o 3 酢酸の酸無水物。 加水分解で酢酸が得られる。 サリチル酸との脱水縮合(エステル化)でアセチルサリチル酸を生じる。 (ch 3 co) 2 o + c 6 h 4 (oh)cooh → c 6 h 4 (ococh 3)cooh + h 2 o アニリンと反応させるとアセトアニリドを生じる。
無水酢酸 chem_idjpn cas rn®1047 化学物質名(和名)無水酢酸 化学物質名(英名)aceticanhydride 分子式c4h6o3 アニリンは、さらし粉で赤紫。 問題文から、白色固体Xと白色固体Yの側鎖を考えてみます。 ということで、呈色反応の組合せは下のようになります。 問5です。 pアミノフェノール 218g に無水酢酸 500g を加えて反応させています。 過不足のチェックです。アニリンのアセチル化の実験を通じて、試薬の調合、吸引沪過、再結晶など、有機化合物の合 成に必要な基本操作を習得する。 2 反応式 ch3c o o cch3 o h n cch3 o ho cch3 o アニリン 無水酢酸 アセトアニリド 酢酸 c c c c c c n c o o c o h h h h h h c h h c h h h h c c c c c
この反応では、無水酢酸のカルボニル基が、サリチル酸の oh 基を引き寄せ、酢酸を追い出します。これまでの例では、カルボン酸から水分子が追い出される反応でしたが、カルボン酸に限らず、この「 引き寄せて 、 追い出す 」のメカニズムにより反応が進行します。 続いて、私たちの身アニリンから pニトロアニリンの合成 アニリンのアミノ基をアセチル基(CH 3CO)で保護してからニトロ化する。ニトロ化の後、加 水分解反応 100 mLのビーカーに無水酢酸ナトリウム約15 g1を入れ、水6 mLを加えて溶解する。別に、 50 mLのビーカーに水25 mLと濃塩酸(12 mol/L)10 mLを加アニリンと無水酢酸が反応すると、アセチル化という現象が起きました。 つまり、アニリンにアセチル基ch 3 coができるわけです。 このとき出来上がる物質は、アセトアニリドでしたね。 構造式は、次のようになります。 アセチル化反応において、アセチル基を提供する反応剤(化合物)の




アニリンと無水酢酸の反応式 アセトアニリド生成 酢酸を使用しない理由は



2
今回行った反応の様子は下記の反応式で示されます。→(矢印)は電子の動きを表しています。 Click ケミストリー ー化学と英語をChem Tutorで プレイヤー智子、築部 浩 共 編 三共出版 電子の動きでみる有機反応のしくみ 奥村 格、杉村 高志 東京化学同人 今回の "実験" はいかがでしたでしょうアセトアニリドは、無水酢酸とアニリンとの間の反応によって製造することができる。しかし、製造時にはアニリンは有毒であり、皮膚を通して吸収される可能性があるため、反応はヒュームフードの下で行われるべきです。 c 6 h 5 nh 2 (ch 3 co) 2 o→c 6 h 5 nhcoch 3 ch 3 cooh アニリンとアニリンと無水酢酸を反応させると,白色の結晶ができましたね。この結晶がアセトアニリドです。アセトアニリドは無色板状結晶です。 それでは,考察です。 アニリンと塩酸の反応を化学反応式で示すと, C 6 H 5NH 2 +HCl→C 6 H 5NH 3 + Cl - アニリン塩酸塩と水酸化ナトリウムの反応を化学



芳香族アミンを網羅的に解説 受験メモ



1
未反応のアニリンが反応する場合は紫色になる。 (4)できたアセトアニリドは回収する。 考察 (1) アニリンと無水酢酸の反応式を書け。 (2) アセトアニリドはアンチフェブリンとも呼ばれる。どのような対症療法作用をもつか。 アニリン 0109mol 無水酢酸 0103mol 溶媒氷酢酸 0174mol 反応式アニリン無水酢酸→アセトアニリド酢酸 この場合、アセトアニリドは何molできますか? 僕は0103molだと考えたのですが、教授はアニリンと氷酢酸が反応するから0109molだと言っています。でもどう融点測定 -アニリンと無水酢酸からアセトアニリドを合成し、再結晶法により精製- 実験日 7月4日金曜日 実験場所 1352材料設計学学生実験室 実験環境 天気:曇り 気温:232℃ 湿度:598% 目的 アニリンと無水酢酸からアセトアニリドを合成し、再結晶法により生成物を精製し、収率を計算する。




大学受験 化学 医薬品に関する問題 広島大学 数学 化学講師 佐藤学による受験生に役立つ濃縮ポイントと Etc



アセトアニリドをアニリンと無水酢酸から合成する実験を行いました そ Yahoo 知恵袋
著者らは無水酢酸の多い系におけるこの反応を高分解能NMRを 用いて追跡した。まず無水酢酸一酢酸系における平衡定数と水酸 基化学シフトの関係式を導き,,40,60℃ で,51,31mol/lを,ま たこれから活性化エネルギーとして46kcal/mol をえた。 つぎに無水酢酸一 酢酸ナトリウムを加えると平衡反応で、アニリンと酢酸が発生する(式2)。 発生したアニリンは、水溶液中の無水酢酸とすぐに反応して した (Scheme 1)。即ち、酢酸中無水酢酸存在下4Bromoindole (1)とdlSerine (2) を反応させると NAcetyltryptophan (3) が得られた。3のAcetylOアセチル化は、塩化アセチルまたは無水酢酸 アミノ基のアセチル化(式(1))は,酢酸ch 3 cooh,無水酢酸(ch 3 co) 2 oまたは酸塩化物 rcoclなどを用いて行われる。アミノ酸などのアミノ基の保護基として用いられることも多いが,アニリンのアセチル化によって得られるアセトアニリドは工業的に



これ おかしくないですか ニトロベンゼンを鈴と塩酸で還元したら Yahoo 知恵袋




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog
抽出し、アニリンは塩酸と反応させることにより抽出する。 cooh na2co3 coona nh 2 nh3cl o h 2 co 2 2 2 hcl また、アセトアニリドの結晶は、アニリンと無水酢酸を反応させることにより得ること ができる。 nh 2 nhcoch 3 (ch3co)2o ch3cooh <2.実験酢酸とアニリンのアミド。 アセチルアニリン、nフェニルアセトアミドともいう。アニリンに無水酢酸あるいは塩化アセチルを反応させて得られる。 無色の板状結晶。 冷水に約05%、熱水には約5%溶ける。 アルコール、クロロホルム、エーテルなどの有機溶媒にはかなり溶けるが、石油にはアセトアニリド (acetanilide) は、アミドの一種で、フレーク状の外見を持つ無色の固体。 Nフェニルアセトアミド、アセタニルなどとも呼ばれる。アンチヘブリンという名称でかつて解熱鎮痛剤として用いられていた有機化合物。 合成 アセトアニリドは、アニリンを無水酢酸と反応させて




芳香族 反応生成物チェック Flashcards Quizlet
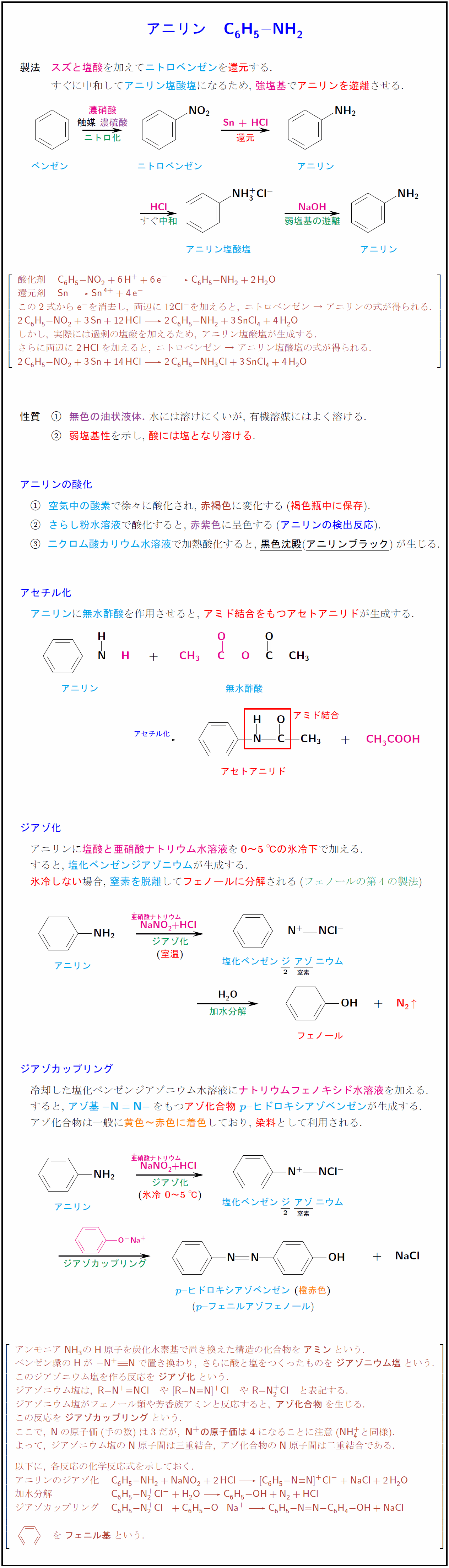



高校有機化学 アニリン C H Nh の製法 酸化 アセチル化 ジアゾ化 ジアゾカップリング 受験の月
化学反応式を考えてみましょう(参考URL ) 無水酢酸が使われるのは、無水酢酸⇒酢酸の反応を利用することによって、アニリンをアセトアニリドにさせるためだと考えられます。 酢酸でも実際にはできることはできると思いますが、反応に時間がかかるのために無水酢酸を利用してい高校化学 主な有機化合物の特徴 (93) 特徴 分子式:C 6 H 7 N ベンゼン にアミノ基が結合した芳香族アミン。 塩基性を示す。 塩酸と反応させると アニリン塩酸塩 を生じる。 C 6 H 5 NH 2 + HCl → C 6 H 5 NH 3 Cl 無水酢酸 と反応させると アセトアニリド を全ての化合物に対して反応性は著しく大である。 二酸化塩素 アンモニア、メタン、ホスフィン、硫化水素 塩素酸塩 アンモニウム塩、酸類、金属粉、硫黄、一般に微粉砕した有機物あるいは可燃 性物質 過塩素酸塩 無水酢酸、ビスマス及びその合金、アルコール、紙、木材 過マンガン酸カ�




アニリンのニトロ化 アニリンをニトロ化する際 直接ニトロ化するので 化学 教えて Goo



質問です 有機化学で このアセトアニリドの共鳴に関する反応機構は正しいでしょう Yahoo 知恵袋




100以上 アニリン 無水酢酸 化学反応式 アニリン 無水酢酸 化学反応式



放課後化学講義室 高校の有機化学は化学的でない
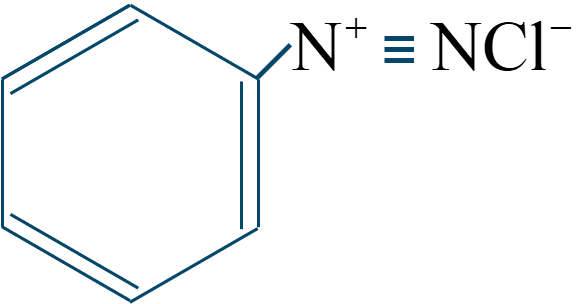



有機化学のまとめと効率的暗記 芳香族アミン ページ 3 耳たこ高校化学暗記帳
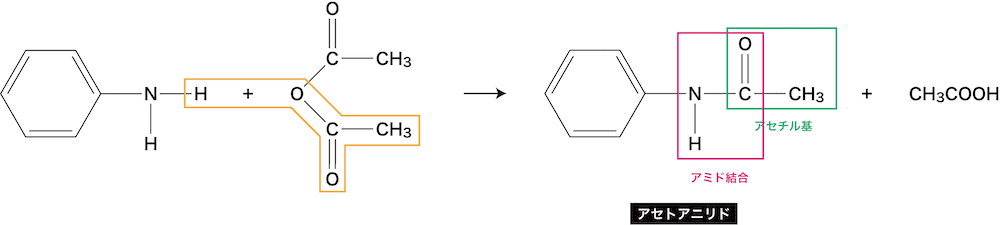



芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ



窒素を含む芳香族化合物




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog



B1v6 Rf8erv55m




融点測定 アニリンと無水酢酸からアセトアニリドを合成し 再結晶法により精製



1




高校化学 アニリンと無水酢酸の反応 練習編 映像授業のtry It トライイット



第137章 医薬品



1



1




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog




アニリン塩酸塩はベンゼンにnh3 とcl なので Clearnote




アニリンの性質とアニリンの反応を徹底的にまとめてみた 化学受験テクニック塾
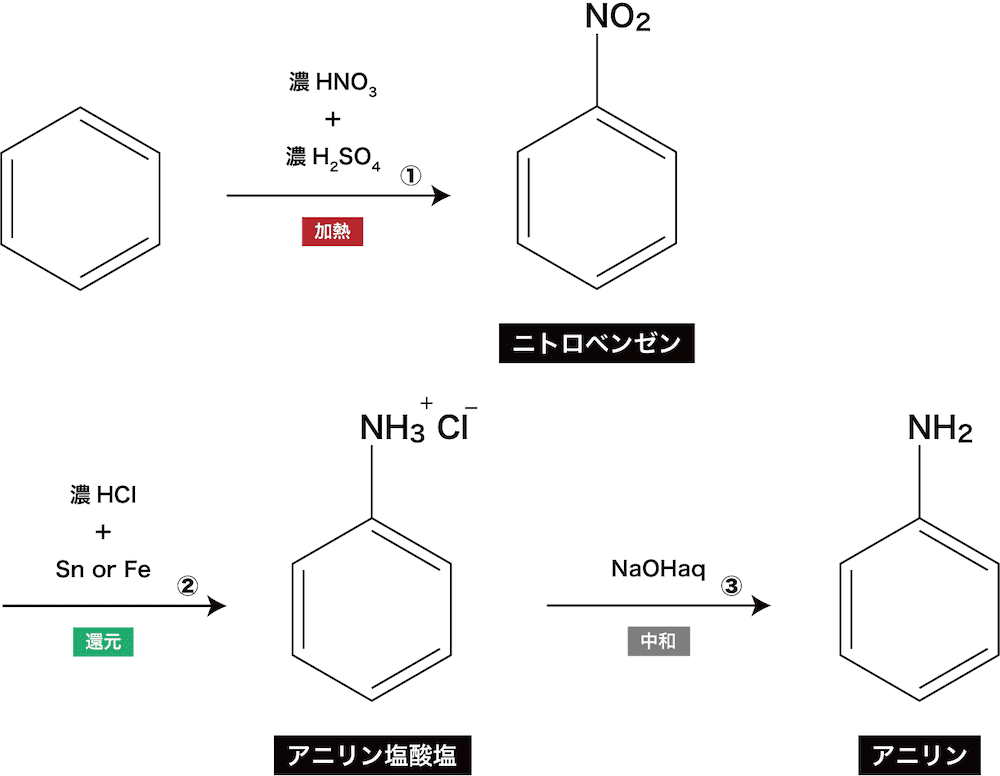



芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ




100以上 アニリン 無水酢酸 化学反応式 アニリン 無水酢酸 化学反応式



P ニトロアセトアニリドからp ニトロアニリンへの反応機構 Okwave



アセチル酸 無水酢酸の反応の中間体の名前が知りたいです どう調べれば良 Yahoo 知恵袋



第137章 医薬品




酢酸と無水酢酸 分子内脱水反応 Irohabook




アセチル化について教えてください ある物質をアセチル化するのに無 化学 教えて Goo



有機反応機構 カルボン酸とその誘導体の反応



1



今日の実験 アセトアニリドの合成 196 の部屋




芳香族 反応生成物チェック Flashcards Quizlet




アセトアニリド Wikipedia




この問題の5でできるアセトアニリドについてですが 解説にはアの操作で分離出来 Clearnote




アニリン 無水酢酸 赤色 アニリン 無水酢酸 赤色 Mbaheblogjpmx2d




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog
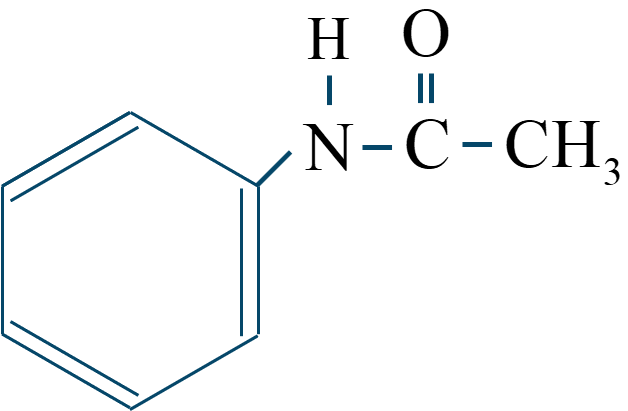



有機化学のまとめと効率的暗記 芳香族アミン ページ 3 耳たこ高校化学暗記帳




アニリン Chemihack おうちで学べる化学
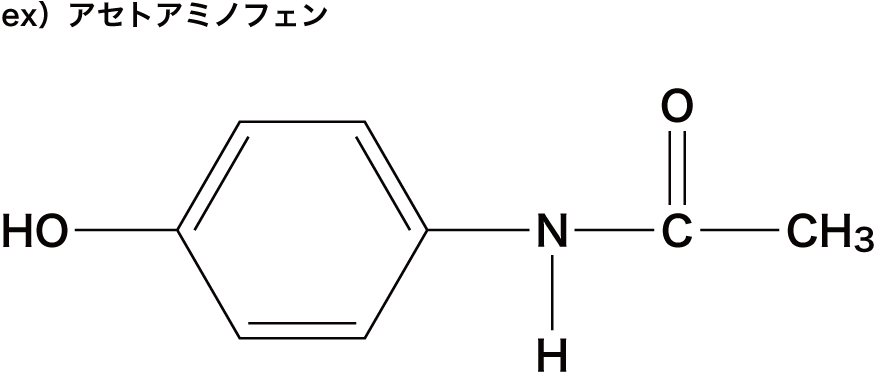



芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ
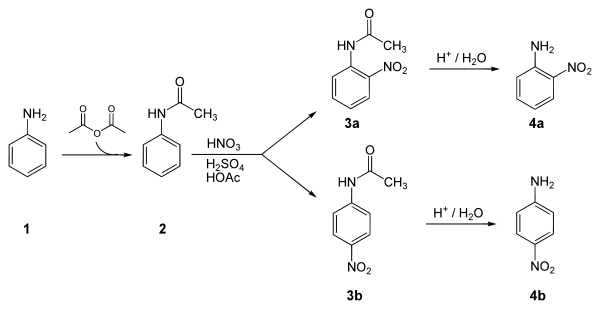



4 ニトロアニリン Wikipedia




高校化学 アニリンブラック 映像授業のtry It トライイット




高等学校化学i 芳香族化合物 アニリンとアゾ化合物 Wikibooks




酢酸エチル Wikipedia



収率の計算はこういうふうにやるのです Life Chemistry




高校化学 アニリンと無水酢酸の反応 映像授業のtry It トライイット




フェノール類とアニリンの呈色反応の語呂合わせ 18h30大学入学共通テスト試行調査第2回第3問b 語呂合わせで高校化学 大学入試ゴロ化学
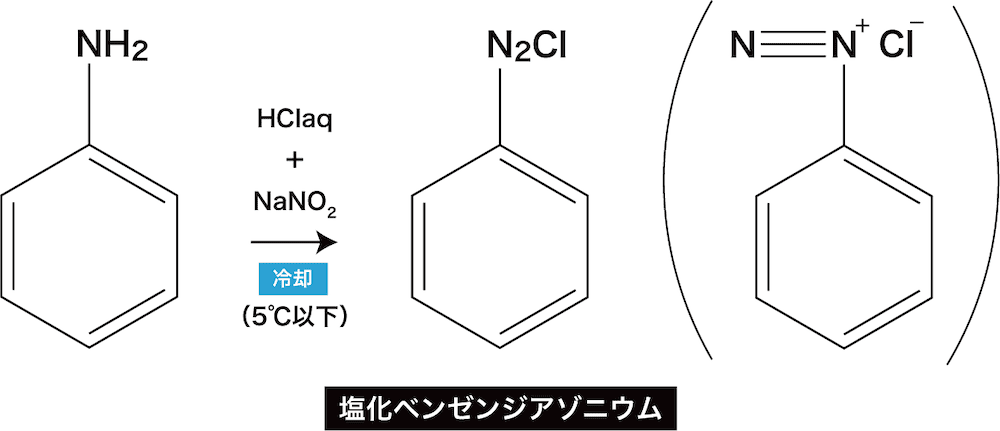



芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ




イソニトリルの合成 アニリン クロロホルム 水酸化ナトリウムを加熱して生 Okwave
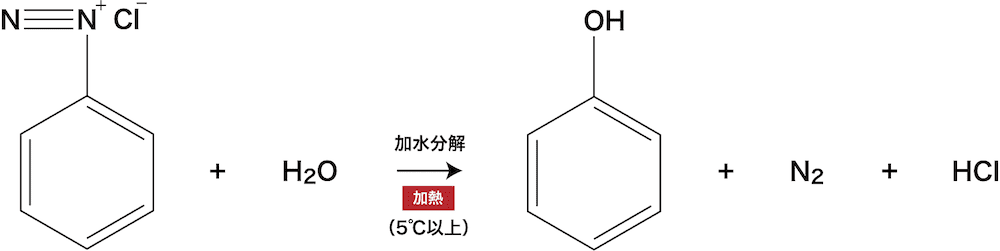



芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ




有機反応を俯瞰する ー縮合反応 Chem Station ケムステ




サリチル酸がアセチル化されアセチルサリチル酸となる反応式
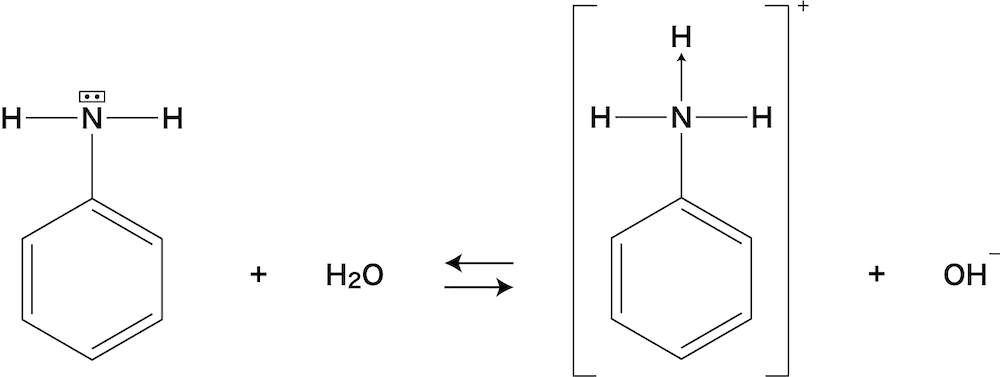



芳香族アミン アニリン の構造 製法 性質 反応 化学のグルメ



窒素を含む芳香族化合物



アニリンからアセトアニリドの反応機構とアセトアニリドからp ニ Yahoo 知恵袋



2




有機反応を俯瞰する ー縮合反応 Chem Station ケムステ




アニリン 合成 化学反応式 アニリン塩酸塩 有機化学 高校化学 エンジョイケミストリー Youtube
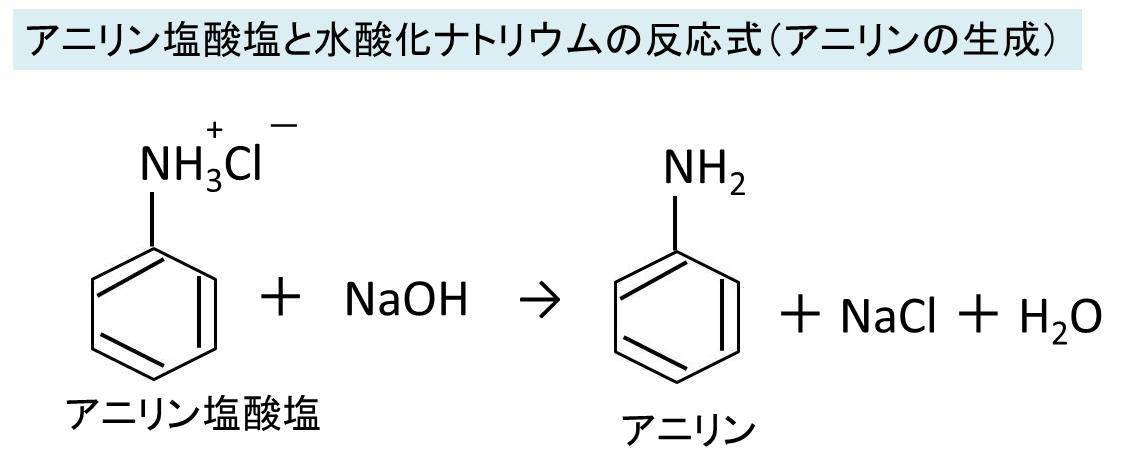



アニリンと塩酸の反応式 アニリン塩酸塩生成 やアニリン塩酸塩と水酸化ナトリウムの反応式



アセトアニリドをニトロ化する際 固体のアセトアニリドに濃硫酸 Yahoo 知恵袋




アセトアニリドの合成 アセトアニリド 再結晶 Tlc 薄層クロマトグラフィー 融点測定 Transblog
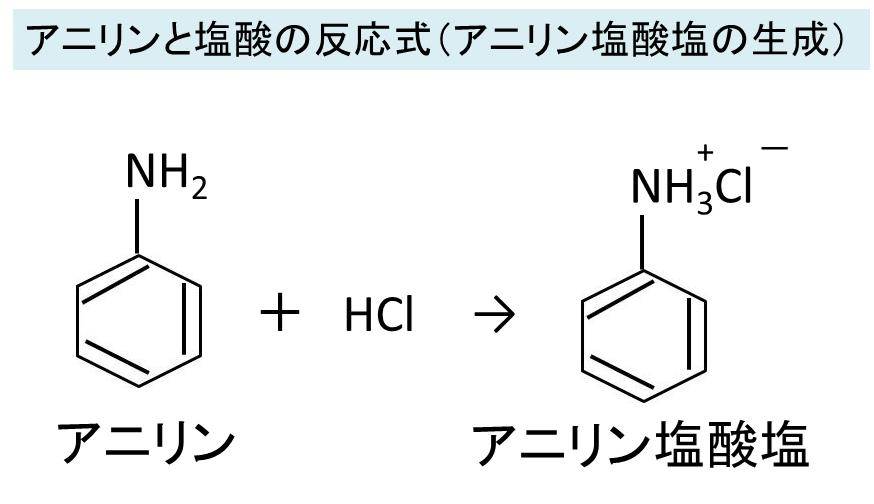



アニリンと塩酸の反応式 アニリン塩酸塩生成 やアニリン塩酸塩と水酸化ナトリウムの反応式
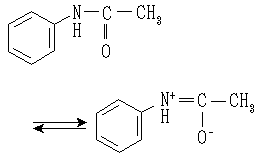



アセトアニリドとは コトバンク
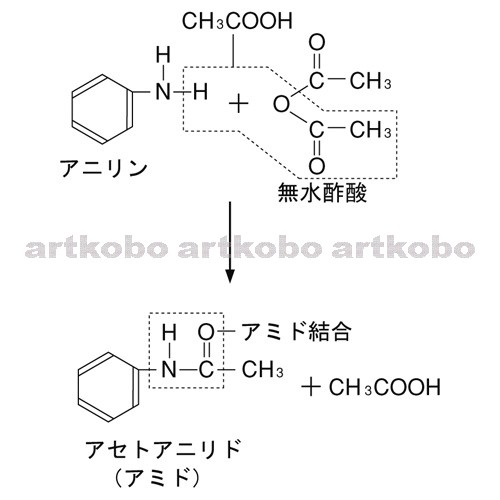



Web教材イラスト図版工房 R Ch 芳香族化合物 56



窒素を含む芳香族化合物



1



求核置換反応についてです 大学の実験でアセトアニリドを合成しました Yahoo 知恵袋



アニリンに無水酢酸を作用させる この時の化学反応式を教えてくださいm Yahoo 知恵袋




100以上 アニリン 無水酢酸 化学反応式 アニリン 無水酢酸 化学反応式
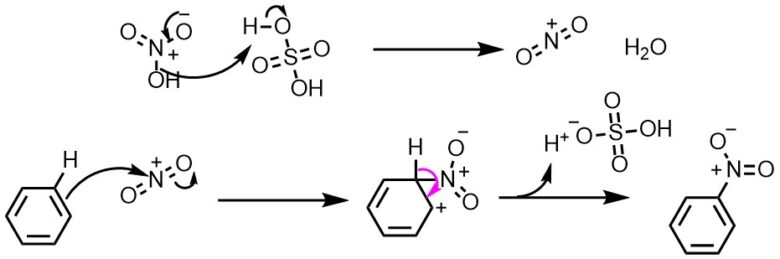



コレクション アニリン 無水酢酸 反応 アニリン 無水酢酸 反応機構



ひたすら受験問題を解説していくブログ14年08月
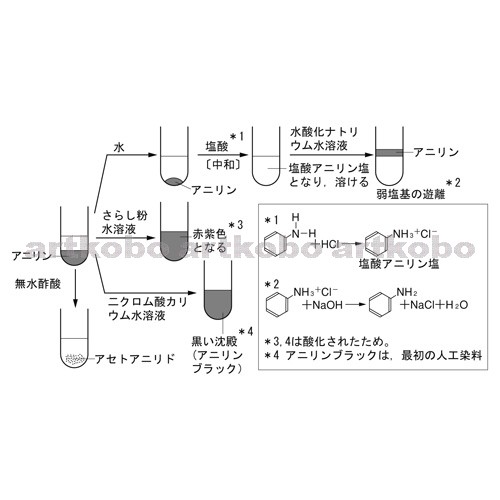



Web教材イラスト図版工房 R Ch 芳香族化合物 52




アニリンの性質と製法 塩化ベンゼンジアゾニウムとpヒドロキシアゾベンゼン Irohabook




フェノール類とアニリンの呈色反応の語呂合わせ 18h30大学入学共通テスト試行調査第2回第3問b 語呂合わせで高校化学 大学入試ゴロ化学




1の2つの反応の反応式教えてください Clear



環化 問6



2




高校化学 アニリンと無水酢酸の反応 映像授業のtry It トライイット



第85章 実験 アニリンとアセトアニリド



カルボニル化合物 カルボン酸誘導体




名城大学理工学部応用化学科 永田研究室 有機化学演習 第10回疑問点など
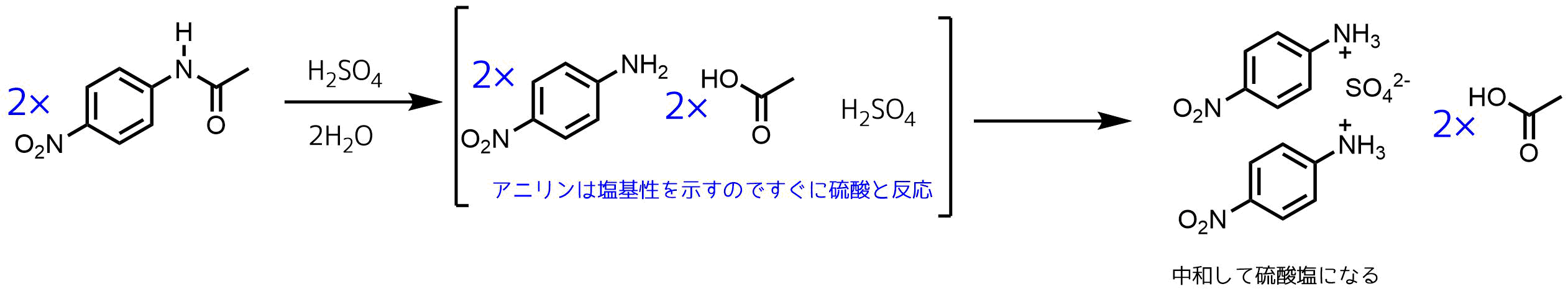



ニトロ化反応の条件とやり方 ネットdeカガク




Wo05 0905号 微生物及び微生物由来酵素によるアニリン誘導体のアセチル化 Astamuse




2 3 アニリンと酢酸の反応



2




有機反応を俯瞰する ー縮合反応 Chem Station ケムステ



医療工学科の化学講義 26 窒素を含む有機化合物 Life Chemistry



芳香族アミンを網羅的に解説 受験メモ




芳香族化合物の質問です Clearnote




4 で 無水酢酸のモルは調べなくても良いのでしょうか Clearnote




4 ジメチルアミノピリジン Wikipedia




高校化学 アニリンと無水酢酸の反応 練習編 映像授業のtry It トライイット




高等学校化学i 芳香族化合物 アニリンとアゾ化合物 Wikibooks




アセチル化について教えてください ある物質をアセチル化するのに無水酢酸 Okwave




アニリン Wikipedia




有機反応を俯瞰する ー縮合反応 Chem Station ケムステ




50 アニリン 無水酢酸 反応機構 アニリン 無水酢酸 反応機構 Mbaheblogjpasjf



第137章 医薬品



0 件のコメント:
コメントを投稿